실험 결과
토의 사항
본 실험은 금속의 부식속도측정 실험이다. 동전 분극에서는 부식속도를 직접 측정하고 타펠상수를 구하는 실험이었고, 선형분극실험은 저항 Rp값을 구하여 동전위에서 구한 타펠 상수를 대입하여 부식속도를 측정하는 것이고, 보데도표는 Rp + Rs값에서 Rs값을 빼서 구한 Rp값에 동전위 실험에서 구한 타펠상수를 대입하여 부식속도를 구하는 실험이었다. 나이퀴스트도표는 보데도표를 이용해 구한 Rp값을 참고하여 그래프를 그려서 결과 값은 보데도표와 같게 나온다.
NaCl 탄소강의 경우는 부식속도가 평균적으로 7.0Х10-5 (A/㎠) 값이 나왔다. 동전위분극과 나이퀴스트, 보데도표의 결과값은 거의 오차가 발생하지 않았다. 하지만 선형분극의 경우는 나머지 값에 비해 오차가 발생하였다.
H2SO4 탄소강의 부식속도는 평균 1.0Х10-3 (A/㎠)이 나왔다. 역시 NaCl 탄소강과 마찬가지로 동전위분극과 나이퀴스트, 보데도표의 결과 값은 거의 오차가 발생하지 않았지만 선형분극에서의 결과에서는 오차가 발생했다.
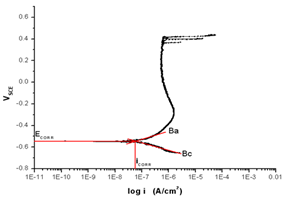
NaCl STS 316L의 부식속도는 평균 6.8Х10-6 (A/㎠)이 나왔다. 실험에서 동전위 분극의 데이터 값이 선형분극, 나이퀴스트도표, 보데도표 보다 정확히 나올 수 밖에 없다. 동전위는 실험에서 나온 결과 값을 바로 읽으면 되지만, 선형분극과 다른 실험은 타펠상수를 사용하여 Stern-Grary equation 계산 과정을 거치기 때문에 상대적으로 부정확할 수 밖에 없다. NaCl STS 316L의 실험의 경우는 동전위에서의 값과 나머지 실험들의 값이 상당히 차이난다.
그 이유가 무엇일까 생각해 봤는데 타펠상수의 값에 문제가 있지 않나 하는 생각이 들었다. 타펠상수의 경우는 그래프의 기울기 인데 그 기울기를 어떻게 그리냐에 따라 결과 값이 달라질 수 밖에 없다. 그래프 기울기가 바뀌면 부식속도의 결과 값 역시 바뀌기 때문에 그래프를 잘못 그렸다는 생각이 든다.
H2SO4 STS 316L의 부식속도는 평균 3.86Х10-6 (A/㎠)이란 결과 값이 나왔다. 3개의 실험에서 모두 비슷한 값이 결과로 나와서 오차 값이 상당히 적었다.
같은 탄소강의 경우는 H2SO4에서의 부식속도가 NaCl에서의 부식속도에 비해 빠르게 부식 됐음을 알 수 있다. 즉 pH가 부식 속도에 영향을 미친다는 것을 알 수 있다. 마찬가지로 같은 STS 316L의 경우도 역시 NaCl에서 보다 H2SO4에서 부식속도가 더 빠른 것을 알 수 있다. 그리고 같은 용액에서 탄소강과 STS 316L의 차이는 탄소강의 훨씬 빨리 부식 됐음을 알 수 있다.
본 실험에서 어려웠던 점은 타펠 기울기를 그리는 작업이었다. 그은 접선이 실제 그래프와 거의 겹치는 경우는 고민을 하지 않아도 되었지만 그렇지 않은 경우는 어디를 기준으로 잡아서 접선을 그어야 되는지 많은 고민을 하게 만들었다. 비교할 수 있는 이론적인 값이라도 있었으면 했지만 도서관도 가보고 인터넷도 뒤져 봤지만 결국은 찾지를 못했다. 지금 한 실험이 정확한 실험이었는지 비교해볼 문헌은 없지만, 같은 시편(아주 조금 다르긴 하지만)을 사용하여 3번을 실험했기 때문에 그래도 어느정도는 정확한 값이 나왔다고 생각한다.































!&emoji=☕&slug=xFu35q9&button_colour=5F7FFF&font_colour=ffffff&font_family=Poppins&outline_colour=000000&coffee_colour=FFDD00)



![[일반생물학실험]온도와 pH가 효소작용에 미치는 영향 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjdvNA5S925m8lScjFhJj-uy5SdCcaNFG1AuR_7BbQbDEoHBDEEkqfM64sipvro3RydmSO4_MS2794o2bJ0FCljQ31pcD5W39ZGOHROD7qKXLO1rlm2ZuBtbxJ9CZHSnsk2v1KSEsL4EGA/w680/%25EC%2598%25A8%25EB%258F%2584%25EC%2599%2580+pH%25EA%25B0%2580+%25ED%259A%25A8%25EC%2586%258C%25EC%259E%2591%25EC%259A%25A9%25EC%2597%2590+%25EB%25AF%25B8%25EC%25B9%2598%25EB%258A%2594+%25EC%2598%2581%25ED%2596%25A5.PNG)
![[일반생물학실험]여러 조건에 따른 효소 반응](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj4kaETe9N8j9q9-ClYy9V1kM2L9s5l19K6YoBOE0SB70BmssQXzVADvQijp1ieiQ9mIxcmCwz9e-YCQFVnXYR7m1vmfjTSs0ZNxCmBLG7wgzRBqiY1Kizx8YuhSdw-RDbs1PohokUd69c/w680/%25EC%2597%25AC%25EB%259F%25AC+%25EC%25A1%25B0%25EA%25B1%25B4%25EC%2597%2590+%25EB%2594%25B0%25EB%25A5%25B8+%25ED%259A%25A8%25EC%2586%258C+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반생물학실험]항생제 감수성 검사 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEhwCJEjB_r2Ojsrn244q-fQmpHsDyUUfgWMUnsfhPKQeN2e7_u1pN_ZuwIdxPLVWS6LFywJUrDTYWJe2V6ZVVb1PtfyvX62Y15OxPfXoiaJkqVoSir3ZoFAmDpe5GcoMBmxEsJUKsSvWYc/w680/%25ED%2595%25AD%25EC%2583%259D%25EC%25A0%259C+%25EA%25B0%2590%25EC%2588%2598%25EC%2584%25B1+%25EA%25B2%2580%25EC%2582%25AC.PNG)
![[고분자공학실험]PMMA 중합 반응 - MMA, AIBN 정제와 PMMA Bulk 중합 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj5hkRZhYWcXolP679_yO0kyP8_R-G9dlTqk5AGEdfsIq9M5K3DJc_tvpYck4x1kciBm2IWwFygrzfWH-HPzUjXiCHAFrjv9zeKYDxAl2tGNqgryyc3t9y4B9lQveS_coAqnmZw4pX4Hyo/w680/PMMA+%25EC%25A4%2591%25ED%2595%25A9+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반화학실험]산화-환원 적정 : 비타민 C의 정량 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEintFUW1pYHbKK8MPzki4vdqVMjTUEFFxPdZB1sTJQw13XSFZWqcN5w0x1AlyzfErlYYSgoNqBni4YGlpFC4ZeULK9VHbhfIXLiuZ3UWTl2oBRua7FE8UUQqtYEx3498FENAnlHlh0f8RFkT7Na8jveOtBtQ5UbY8jE80ZCwFoU_jqw_0Z6BofRYZF7/w680/%EC%82%B0%ED%99%94-%ED%99%98%EC%9B%90%20%EC%A0%81%EC%A0%95%20-%20%EB%B9%84%ED%83%80%EB%AF%BC%20C%EC%9D%98%20%EC%A0%95%EB%9F%89.PNG)
0 댓글