실험 결과
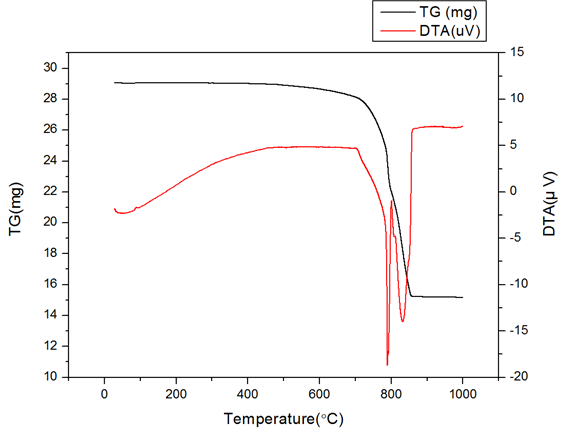
TGA곡선의 변화는 온도가 730℃부근에서 30㎎중량이 점점 줄어들기 시작하더니 15㎎정도까지 줄어드는데 처음에는 MgCO3에서 MgO+CO2로 분해가 되는 과정이고 이어서 850℃정도에서 CaCO3가 CaO+CO2로 분해가 되면서 질량이 줄어든다. 원래는 2번의 질량 변화가 일어나야 하는데 승온 속도가 빠르게 올라가면서 한번으로 보이게 된거 같다. DTA곡선의 변화는 열량이 700℃부근에서 MgO+CO2로 분해가 되면서 첫 번째 흡열 픽이 발생하고 820℃부근에서 CaCO3가 CaO+CO2로 분해하면서 두 번째 흡열 픽이 발생하게 된다.
토의 사항
MgCO3․CaCO3는 열이 증가함에 따라서 CO2가 분자상태에서 떨어져 나오면서 흡열 반응이 발생을 하게 된다. 이에 MgCO3․CaCO3는 CaO와 MgO에 CO2가 결합이 되 있어서 결합력이 더 낮은 것 같다.
2. 질문 사항
1) dolomite의 분해반응 (MgCO3․CaCO3→MgO+CO2+CaO+CO2)을 이용하여, 각 성분의 분자량을 기준으로 이론적은 무게의 감소량을 계산한다.
분자량 ㎎=24.3g/㏖ Ca=40g/㏖ O=16g/㏖ C=12g/㏖
MgCO3는 24.3g+12g+(16g×3)=84.3g CaCO3는 40g+12g+(16g×3)=100g
CO2는 12g+(16g×2)=44g 2CO2는 44g×2=88g
88g/(84.3g+100g)×100 = 48%
20㎎×0.48=9.6㎎
2) DTA-TGA결과와 이론적인 무게 감소량을 비교한 후, 각 성분의 정확한 분해온도를 결정한다.
원래는 MgCO3․CaCO3를 20㎎을 넣었지만 그래프대로 계산을 해보면 29㎎×0.48=13.92g이 줄어들고 15.08㎎이 남아야 되는데 실제로도 약15㎎이 남았다. 실제 양과 비슷한 양의 CO2가 날아갔다. 흡열 peak의 최하인 부분을 보면 790℃와 830℃이다.
3) 분해과정에서 DTA곡선에 나타나는 발열 도는 흡열 Peak의미를 설명한다.
LLDPE의 온도상승 온도 냉각 재가열인데 앞부분 처럼 Peak가 아래로 내려갈 경우 흡열 Peak로 α-Al2O3와 MgCO3․CaCO3의 온도 차이가 나면서 흡열일 경우 주위에 열을 흡수하면서 Reference의 온도가 낮아지면서 온도를 맞추기 위해 전기를 α-Al2O3에 가해지면서 Peak가 낮아지고 발열 Peak는 Peak가 위로 올라가는 것으로 MgCO3․CaCO3가 발열을 하면서 Reference의 온도가 높아지면서 온도를 맞추기 위해 MgCO3․CaCO3에 전기를 가하면서 Peak가 높아진다.
4) 세라믹스원료로 사용하기 전에, 원료를 분해시켜 가스를 제거하는 공정을 무엇이라 부르는가?
하소: 하소는 광석 등의 고체를 가열하여 열분해나 상전이를 일으키거나 휘발 성분을 제거하는 열처리 과정이다. 일반적으로 제품 물질의 녹는점 이하의 온도에서 진행하여 원하는 재료를 얻는 과정이다.



!&emoji=☕&slug=xFu35q9&button_colour=5F7FFF&font_colour=ffffff&font_family=Poppins&outline_colour=000000&coffee_colour=FFDD00)



![[일반생물학실험]온도와 pH가 효소작용에 미치는 영향 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjdvNA5S925m8lScjFhJj-uy5SdCcaNFG1AuR_7BbQbDEoHBDEEkqfM64sipvro3RydmSO4_MS2794o2bJ0FCljQ31pcD5W39ZGOHROD7qKXLO1rlm2ZuBtbxJ9CZHSnsk2v1KSEsL4EGA/w680/%25EC%2598%25A8%25EB%258F%2584%25EC%2599%2580+pH%25EA%25B0%2580+%25ED%259A%25A8%25EC%2586%258C%25EC%259E%2591%25EC%259A%25A9%25EC%2597%2590+%25EB%25AF%25B8%25EC%25B9%2598%25EB%258A%2594+%25EC%2598%2581%25ED%2596%25A5.PNG)
![[일반생물학실험]여러 조건에 따른 효소 반응](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj4kaETe9N8j9q9-ClYy9V1kM2L9s5l19K6YoBOE0SB70BmssQXzVADvQijp1ieiQ9mIxcmCwz9e-YCQFVnXYR7m1vmfjTSs0ZNxCmBLG7wgzRBqiY1Kizx8YuhSdw-RDbs1PohokUd69c/w680/%25EC%2597%25AC%25EB%259F%25AC+%25EC%25A1%25B0%25EA%25B1%25B4%25EC%2597%2590+%25EB%2594%25B0%25EB%25A5%25B8+%25ED%259A%25A8%25EC%2586%258C+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반생물학실험]항생제 감수성 검사 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEhwCJEjB_r2Ojsrn244q-fQmpHsDyUUfgWMUnsfhPKQeN2e7_u1pN_ZuwIdxPLVWS6LFywJUrDTYWJe2V6ZVVb1PtfyvX62Y15OxPfXoiaJkqVoSir3ZoFAmDpe5GcoMBmxEsJUKsSvWYc/w680/%25ED%2595%25AD%25EC%2583%259D%25EC%25A0%259C+%25EA%25B0%2590%25EC%2588%2598%25EC%2584%25B1+%25EA%25B2%2580%25EC%2582%25AC.PNG)
![[고분자공학실험]PMMA 중합 반응 - MMA, AIBN 정제와 PMMA Bulk 중합 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj5hkRZhYWcXolP679_yO0kyP8_R-G9dlTqk5AGEdfsIq9M5K3DJc_tvpYck4x1kciBm2IWwFygrzfWH-HPzUjXiCHAFrjv9zeKYDxAl2tGNqgryyc3t9y4B9lQveS_coAqnmZw4pX4Hyo/w680/PMMA+%25EC%25A4%2591%25ED%2595%25A9+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반화학실험]산화-환원 적정 : 비타민 C의 정량 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEintFUW1pYHbKK8MPzki4vdqVMjTUEFFxPdZB1sTJQw13XSFZWqcN5w0x1AlyzfErlYYSgoNqBni4YGlpFC4ZeULK9VHbhfIXLiuZ3UWTl2oBRua7FE8UUQqtYEx3498FENAnlHlh0f8RFkT7Na8jveOtBtQ5UbY8jE80ZCwFoU_jqw_0Z6BofRYZF7/w680/%EC%82%B0%ED%99%94-%ED%99%98%EC%9B%90%20%EC%A0%81%EC%A0%95%20-%20%EB%B9%84%ED%83%80%EB%AF%BC%20C%EC%9D%98%20%EC%A0%95%EB%9F%89.PNG)
0 댓글