실험 목적
염료 및 유기안료 중에 가장 큰 비율을 차지하고 있는 디아조화합물의 제조에 있어서 디아조화 및 짝지음 반응은 대단히 중요하다. 본 실험에서는 디아조화와 짝지음 반응에 의하여 염료를 합성함과 동시에 이 반응에 미치는 여러 가지 조건을 검토한다. 또한 이들 반응의 염색에의 응용을 통하여 저분자물이 고분자 화합물에 흡착되는 과정에 관하여 관찰한다.
실험 이론 및 원리
방향족 1차 아민(Ar-NH3)에 염산의 존재 하에서 아질산(HNO2)을 반응시키면 디아조늄염(Ar-N2Cl)을 생성한다.
이 디아조화 반응의 일반적인 방법으로서는 아민 1몰을 약 10배 양의 H2O와 약 2.5몰의 염산에 용해시키고 얼음으로 냉각하여 0℃근처에서 교반하면서 계산양의 아질산소다(NaNO2)수용액을 가한다. 그러나 sulfanilic acid와 같이 SO3H 염을 가지며 물과 염산에 거의 녹지 않는 아민을 디아조화 할 경우에는 가성소다 또는 탄산소다를 사용하여 물에 녹이고 이것에 NaNO2를 가한 용액을 묽은 염산 중에 주입시켜 디아조화를 행한다. 또 염기성이 극히 작고 염산에 용해하지 않는 아민은 이것을 conc H2SO4 중에 녹여서 nitrosile sulfuric acid를 사용하여 디아조화 할 경우도 있다.
이때 사용되는 산은 염산이나 황산이 상용되며 염산의 경우 아미노기 한 개에 대해 이론적으로 두 당량을 요하나 실제로는 0.2~0.5당량 과잉인 2.2~2.5당량을 요한다. 이것은 아질산의 이온 해리를 막고, 생성한 아민염의 가수분해를 억제하며, 생성한 디아조늄염과 원료 아민과의 짝지음을 막기 위한 것이다. 또한 디아조늄염은 대단히 불안정하므로 낮은 온도(0~5℃)에서 실시한다.
방향족 디아조늄이온은 저온에서는 조금 안정하나 온도가 올라가면 불안정하여 질소(N2)가 떨어지면서 다른 치환기로 치환된다. 수용액에서 가열하면 가수분해가 일어나서 -OH기가 치환된다. 디아조늄기를 Cu2(CN)2, Cu2Cl2, Cu2Br2 시약으로 처리하여 -CN, -Cl, -Br기를 치환시키는 반응을 Sandmeyer반응이라고 하며 -F기를 도입시키는 반응을 Schiemann반응이라고 한다.
2. 짝지음
디아조늄염은 일반적으로 반응성이 크므로, 저온에서도 다른 방향족 아민류, 페놀류 등과 각각 산성 및 알칼리성에서 반응시켜 짝지음을 일으키고 아조 화합물을 생성한다.
예를 들면,
여기서 디아조늄염을 만드는 아민류를 짝지음 성분이라 한다.
짝지음은 디아조늄염을 다음과 같은 화합물에 반응시켜 아조 화합물을 생성하는 반응을 말한다. 즉 aniline, naphthyl amine 및 이들의 유도체, 또는 페놀, 나프톨 및 이들 유도체(방향족 -NH2, -OH기를 가진 화합물)와의 반응에서 아조화합물(또는 아조염료)을 생성하는 반응을 말하고 반응 위치는 -NH2나 -OH기에 대해 파라 위치에 작용하고 파라가 차 있든지 입체장애(혹은 공간장애)가 있을 때는 오르토위치에 반응한다.
공업적으로 아조염료 제조의 한 공정으로 디아조늄이온을 친전자성 시약으로 반응하여 아조기(-N=N-)를 갖는 화합물을 생성하는 친전자성 방향족 치환반응을 하는데 이때 방향족은 활성화기를 갖고 있어야만 된다. 이 반응을 디아조짝지음 반응 이라고 한다.
디아조 짝지음은 페놀성의 -OH기와 황산, 그리고 카르복실기의 탈 양성자화가 친전자성 방향족 치환에 대해 방향족 고리를 활성화하기 때문에 주로 염기용액에서 일어난다. 대부분의 아조 염료는 물에 대한 용해도를 촉진시키고 면이나 양털 같은 섬유의 극성 표면에 염료의 결합을 돕기 위해 분자에 하나 이상의 술폰기(-SO3-)나 카르복실기(-COO-)를 가지고 있다.
디아조늄염은 일반적으로 반응성이 크므로 저온에서도 다른 방향족 아민류, 페놀류 등과 각각 산성 및 알칼리성에서 반응시켜 짝지음을 일으키고 아조화합물을 생성한다. 이때, 디아조늄염을 만드는 아민류를 짝지음 성분이라고 한다. 디아조늄 이온은 약한 친전자체이다. 그들은 아주 반응성이 큰 방향족 화합물(페놀이나 3차 아릴아민)과 반응하여 아조 화합물을 만든다. 이러한 친전자성 방향족 치환반응을 디아조 짝지음 반응이라고 한다.
디아조늄 양이온과 페놀 사이의 짝지음 반응은 약알칼리성 용액에서 가장 잘 일어난다. 이 조건하에서 상당량의 페놀이 페녹시화이온, ArO-로 존재하며, 페녹시화이온은 페놀 자체보다 친전자성 치환반응을 더욱 잘 한다. 용액이 너무 알칼리성이면 디아조늄염 자체가 수산화이온과 반응하여 비교적 반응이 작은 디아조히드록시드 또는 디아조트산이온이 만들어진다.
Ar-N+≡N: | OH- ⇄ H+ | Ar-N"=N"-OH | OH- ⇄ H+ | Ar-N"=N"- - |
arenediazonium ion (짝짓는다) | | diazohydroxide (짝짓지않는다) | | diazoate ion (짝짓지않는다) |
디아조늄 양이온과 아민사이의 짝지음반응은 약산성 용액에서 가장 신속히 일어난다. 이 조건에서 디아조늄염의 농도는 최대가 되고 동시에 과량의 아민은 반응성이 없는 아미늄염으로 전환되지 않은 채로 있다.
용액의 pH가 5이하이면 아민의 짝지음 속도는 느리다.
아조화합물은 대개 진한색을 띠고 있다. 왜냐하면 아조결합이 두 방향족고리를 짝짓게 만들기 때문이다. 이것은 비편재화된 π전자의 연장된 계가 되며 가시광선 영역에서 빛을 흡수하도록 한다. 아조 화합물은 짙은 색 때문에 그리고 비교적 값싼 화합물로부터 합성될 수 있기 때문에 염료로 널리 사용된다.
3. 나프톨 염색
디아조화 및 짝지음 반응을 염색과정에서 응용한 실례로서의 나프톨 염색은 특수한 염색법이긴 하지만 셀룰로오스 섬유 등의 염색에 널리 사용되고 있다. 우선 Naphthol AS류를 가성소다용액에 용해하고 이 용액에 섬유를 침투하여 미리 짝지음 성분을 섬유에 흡착시켜 놓는다. 다음에 base류를 디아조화한 디아조늄염 용액 속에 이 섬유를 넣고 짝지음 반응을 일으켜 섬유상에서 염료를 합성한다.
짝지음 성분과 디아조성분의 조합에 따라 각종, 특히 적색의 염색이 가능하다. 또한 끝으로 섬유의 표면에 묻은 염료를 씻어버리고, 특히 마찰 견뇌도를 향상시키기 위하여 soaping을 한다. 이때 견뢰도란, 염색물의 염색 가공공정 또는 그 후의 사용 중에 미치는 작용에 대한 염색물의 색의 저항성을 말한다.
실험 기구 및 시약
1. 실험 기구
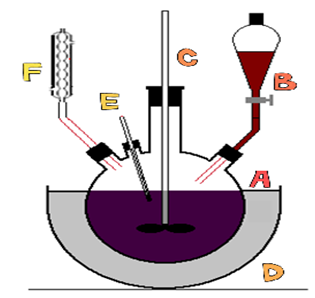
A : 4구 플라스크 | |
B : 물중탕 또는 모래중탕 | |
C : 냉각기 | |
D : 교반기 | |
E : 분액깔때기 | |
F : 온도계 |
2. 실험 시약
1) 나프톨
나프탈렌의 수소원자 하나를 하이드록시기로 치환한 구조를 갖는 화합물이다. 염료의 중요한 중간체로서 분자식 C10H8O. α-나프톨 및 β-나프톨의 두 이성질체가 있다. 페놀과 비슷한 성질을 가지고 있으며, 콜타르 속에 소량 함유되어 있다. 나프톨을 제조하는 데는 대응하는 나프탈렌설폰산을 알칼리 융해시키거나, 나프틸아민을 묽은 황산과 가열하여 아미노기를 하이드록시기로 치환시켜 준다. 염료의 중요한 중간체이다.
α-나프톨은 무색의 막대 모양 결정으로서 염화철(Ⅲ)에 의해 보라색을 나타내므로 철(Ⅲ)이온을 검출하는 데 쓰인다. 한편, β-나프톨은 무색 또는 노란색을 약간 띤 판 모앵 또는 나뭇잎 모양 결정으로서 염화철(Ⅲ) 이온에 의해 녹색을 띤다. 고무의 산화방지제나 연고 등으로 쓰인다.
2) 로우드액
3) 아질산나트륨
화학식 NaNO2, 분자량 69.0, 녹는점 271℃이며, 320℃ 이상에서 분해된다. 조해성이 있으나 아질산칼륨 정도는 아니다. 수용액은 약한 알칼리성을 띤다. 질산나트륨을 납과 함께 녹여 만든다. NaNO3+Pb → NaNO2+PbO 유기아민을 디아조화하는 작용이 있고, 혈관확장작용이 있다. 아질산나트륨은 고기에 함유되어 있는 미오글로빈이나 헤모글로빈과 결합하여 일산화질소 미오글로빈이나 일산화질소 헤모글로빈이 되어 육가공품의 빛깔을 복숭아 빛으로 만든다. 아질산염은 독성이 강하므로 그 사용한도가 식품위생법에 의해 규제되어 있다. 염료의 제조, 육가공품의 염지제, 의약품 등으로 사용된다.
4) 초산나트륨
아세트산과 나트륨이 만드는 염으로, 화학식 을 갖는 약한 산과 강한 염기가 만든 염인데, 그 수용액은 약한 알칼리성을 보이며 화학식은 CH3CO2Na 이다. 분자량은 82.04이며, 녹는점은 324℃이고, 비중은 1.528이다. 약산인 아세트산을 강염기인 수산화나트륨과 반응시키면 중화반응이 일어나 물이 생기고, 아세트산나트륨이 만들어진다. 그 반응식은 다음과 같다.
CH3COOH + NaOH → H2O + CH3COONa
이렇게 하여 얻은 아세트산나트륨은 물 속에서 아세트산이온(CH3COO-)과 나트륨이온(Na+) 상태로 존재하는데, 이 용액을 증발시키고 농축하여 냉각시키면 3수화염인 CH3CO2Na·3H2O가 생긴다. 이 3수화염의 결정을 120∼250℃에서 가열하면 물이 모두 빠져나가 무수염이 된다. 3수화염이나 무수염은 둘 다 바늘 모양의 무색 결정이며, 물에는 잘 녹지만 유기용매에는 거의 녹지 않는다. 약한 산과 강한 염기가 만드는 염이므로 수용액은 약한 알칼리성을 보인다. 아세트산나트륨은 융해열이 크기 때문에 난방기구의 보온재로 사용되기도 한다.







!&emoji=☕&slug=xFu35q9&button_colour=5F7FFF&font_colour=ffffff&font_family=Poppins&outline_colour=000000&coffee_colour=FFDD00)



0 댓글