작용기의 종류와 성질 - 3
4 유기산 및 에스테르류
유기산은 카르복시기(-COOH)를 갖는다. 가장 간단한 것은 포름산(HCO2H)이다. 카르복시기 안에 있는 2개의 산소원자들이 같은 탄소원자에 결합되어 있기 때문에 O-H결합의 극성이 매우 크다. 카르복시산은 수소결합에 의하여 회합하려는 경향이 있다. 또한 산성을 나타내는 양성자는 쉽게 물과 같은 염기들에 제공된다.

양성자전달반응이 쉽게 진행되는 것은 이때 생기는 음이온(RCO2-)이 2개의 동등한 산소원자를 포함하는 공명에 의하여 안정화되기 때문이다.

카르복시기에 인접한 탄소에 붙은 1개의 수소원자 대신에 1개의 할로겐원자가 치환되면 산의 세기는 할로겐치환기의 전기음성도와 대체로 비슷한 세기로 증가한다. 몇 가지 치환된 아세트산의 산성도(acidity)를 표 1에서 비교하였다. 할로겐원소들과 같은 전자음성기(electronegative group)에는 전자 끄는(electron-withdrawing)의 유도효과(inductive effect)가 있다.
 |
| 표 1 몇 가지 치환된 아세트산의 pKa 값 |
이러한 산의 음이온은 치환되지 않은 산의 음이온보다 안정성이 더 큰데 그것은 전자를 잡아당기는 전기음성기의 유도효과에 의하여 생기는 쌍극자의 정전기적 인력 때문이다. 쌍극자의 정전기적 인력 때문이다.
쌍극자에 의하여 1개의 탄소원자에 있는 음전하가 감소하면 인접하고 있는 카르복시산기에 채워진 음전하를 안정화시킨다.

만일 탄소원자에 붙어있는 기가 탄소보다 더 작은 전기음성도를 가지고 있으면 그 기는 전자-방출효과(electron-releasing effect)를 나타낸다. 이것은 산소원자의 전자밀도를 증가시키며 그 결과 산의 세기가 감소된다. 트리메틸규소기(trimethylsilicon group)(CH3)3Si-는 전자 주는 기의 한 예이다.

에스테르류는 하나의 산 RCO2H이 하나의 알코올 R‘OH와 반응하여 만들어 내는 생성물이다. 여기서 기호 R과 R'는 두 알킬기들이 서로 다를 수도 있다는 것을 뜻한다.
![]()
예를 들면 에스테르분자의 구조는 그 모체인 산과 그 모체인 알코올의 두 가지 구조의 특성을 모두 지닌다.
5 아민류
아민류는 암모니아의 유도체라고 생각할 수 있다. 만일 암모니아에 있는 수소원자들 중에서 1개, 2개 또는 3개가 R기로 치환되면 각각 1차, 2차 및 3차 아민류가 된다. 여기서 주의해야 할 점은 아민류에서 1차, 2차 및 3차라 함은 질소 원자에 직접 붙어 있는 탄소원자의 수를 말한다는 사실이다.
한편 암모늄이온(NH4+)과 유사하게 4차아민(NR4+)도 존재하며 이 화합물에서는 암모늄이온의 4개의 수소원자가 모두 R기로 치환되었다. 이러한 모든 화합물에서 질소원자는 sp3형의 혼성궤도 함수에 의하여 σ결합을 형성한다.
한편 방향족 아민류에는 두 가지 형태가 있다. 첫 번째 형은 암모나이 중의 1개의 수소원자가 방향족 원자단으로 치환되어 생긴 화합물이다. 아닐린은 바로 이 유형의 화합물의 가장 간단한 예이다. 두 번째 형의 방향족 아민은 질소원자가 고리구조에 절대로 필요한 한 부분이다. 예를 들면 피리딘(C5H5N)은 그림 1에서 보는 바와 같이 6원자방향족 고리를 완성하는 질소원자를 포함하고 있다.
1개의 질소원자는 CH원자단과 등전자 구조를 이룬다. 그러므로 1개의 질소원자가 방향족 고리에 있는 CH원자단과 치환되면 비편재화된 π결합이 지속된다. 이 경우에 질소원자가 갖는 3개의 sp2 혼성궤도함수 중에서 2개는 인접되어 있는 2개의 탄소원자와 σ 결합을 형성하고 세 번째의 sp2 혼성궤도 함수는 고립전자쌍을 수용한다. 이때 비혼성화된 p궤도함수는 평면고리에서 비편재화된 π결합부분을 형성한다.
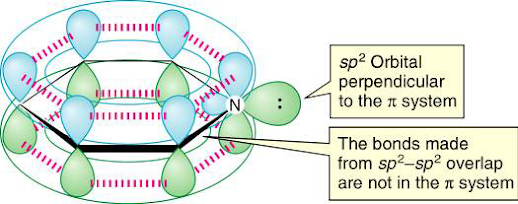 |
| 그림 1 피리딘의 구조 |
질소 원자에 있는 고립전자쌍 때문에 아민류는 양성자 주게(proton donor)와 다른 Lewis산에 대하여 염기성이다. 아민류는 물보다 더 센 염기이며, 수용액에서는 반응하여 짝산과 수산화이온을 만든다.
약한 염기성인 아민류와는 아주 달라서 4차 암모늄수산화물(NR4-OH-)은 OH-이온이 존재하기 때문에 센 염기성을 나타낸다.


!&emoji=☕&slug=xFu35q9&button_colour=5F7FFF&font_colour=ffffff&font_family=Poppins&outline_colour=000000&coffee_colour=FFDD00)



![[일반생물학실험]온도와 pH가 효소작용에 미치는 영향 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjdvNA5S925m8lScjFhJj-uy5SdCcaNFG1AuR_7BbQbDEoHBDEEkqfM64sipvro3RydmSO4_MS2794o2bJ0FCljQ31pcD5W39ZGOHROD7qKXLO1rlm2ZuBtbxJ9CZHSnsk2v1KSEsL4EGA/w680/%25EC%2598%25A8%25EB%258F%2584%25EC%2599%2580+pH%25EA%25B0%2580+%25ED%259A%25A8%25EC%2586%258C%25EC%259E%2591%25EC%259A%25A9%25EC%2597%2590+%25EB%25AF%25B8%25EC%25B9%2598%25EB%258A%2594+%25EC%2598%2581%25ED%2596%25A5.PNG)
![[일반생물학실험]여러 조건에 따른 효소 반응](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj4kaETe9N8j9q9-ClYy9V1kM2L9s5l19K6YoBOE0SB70BmssQXzVADvQijp1ieiQ9mIxcmCwz9e-YCQFVnXYR7m1vmfjTSs0ZNxCmBLG7wgzRBqiY1Kizx8YuhSdw-RDbs1PohokUd69c/w680/%25EC%2597%25AC%25EB%259F%25AC+%25EC%25A1%25B0%25EA%25B1%25B4%25EC%2597%2590+%25EB%2594%25B0%25EB%25A5%25B8+%25ED%259A%25A8%25EC%2586%258C+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반생물학실험]항생제 감수성 검사 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEhwCJEjB_r2Ojsrn244q-fQmpHsDyUUfgWMUnsfhPKQeN2e7_u1pN_ZuwIdxPLVWS6LFywJUrDTYWJe2V6ZVVb1PtfyvX62Y15OxPfXoiaJkqVoSir3ZoFAmDpe5GcoMBmxEsJUKsSvWYc/w680/%25ED%2595%25AD%25EC%2583%259D%25EC%25A0%259C+%25EA%25B0%2590%25EC%2588%2598%25EC%2584%25B1+%25EA%25B2%2580%25EC%2582%25AC.PNG)
![[고분자공학실험]PMMA 중합 반응 - MMA, AIBN 정제와 PMMA Bulk 중합 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj5hkRZhYWcXolP679_yO0kyP8_R-G9dlTqk5AGEdfsIq9M5K3DJc_tvpYck4x1kciBm2IWwFygrzfWH-HPzUjXiCHAFrjv9zeKYDxAl2tGNqgryyc3t9y4B9lQveS_coAqnmZw4pX4Hyo/w680/PMMA+%25EC%25A4%2591%25ED%2595%25A9+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반화학실험]산화-환원 적정 : 비타민 C의 정량 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEintFUW1pYHbKK8MPzki4vdqVMjTUEFFxPdZB1sTJQw13XSFZWqcN5w0x1AlyzfErlYYSgoNqBni4YGlpFC4ZeULK9VHbhfIXLiuZ3UWTl2oBRua7FE8UUQqtYEx3498FENAnlHlh0f8RFkT7Na8jveOtBtQ5UbY8jE80ZCwFoU_jqw_0Z6BofRYZF7/w680/%EC%82%B0%ED%99%94-%ED%99%98%EC%9B%90%20%EC%A0%81%EC%A0%95%20-%20%EB%B9%84%ED%83%80%EB%AF%BC%20C%EC%9D%98%20%EC%A0%95%EB%9F%89.PNG)
0 댓글