효소의 반응특성 - 3
8) 효소반응의 저해
효소와 가역적 또는 비가역적으로 결합하여 효소의 촉매작용을 억제하는 물질을 효소 저해제(enzyme inhibitor)라 한다.
• 비가역적 저해(irreversible inhibition)
저해제가 효소의 활성과 관련이 있는 특정한 원자단이나 활성부위 근처의 아미노산 잔기에 비가역적으로 공유결합함으로써 효소와 기질이 결합할 수 없게 하여 효소의 작용을 방해하는 경우이다. 화학반응으로만 저해제가 제거될 수 있으며 속도론적으로는 비경쟁적 저해로 된다.
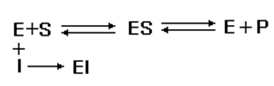
비가역적 효소저해제에는 단순히 효소단백질을 화학적으로 수식하여 효소의 촉매작용에 필수적인 부위를 막거나 기질과의 결합을 입체적으로 저해하는 화학수식제와 활성부위 지향성 비가역 저해제(active-site-directed irreversible inhibitor), 그리고 효소의 활성부위 또는 그 근방의 무극성부위에 결합하거나 활성부위를 알킬화하는 친화성 표지시약(affinity labeling reagents) 등이 있다 .
• 가역적 저해(reversible inhibition)
효소의 어떤 결합부위에 저해제가 가역적으로 결합하여 효소의 작용을 저해한다.
- 경쟁적 저해
경쟁적 저해(competitive inhibition)는 기질과 저해제의 화학구조가 비슷하여 효소단백질의 활성중심에 대하여 저해제가 기질과 경쟁적으로 비공유결합하여 효소의 작용을 저해하는 것이다. 이 효소반응에서 기질농도 [S]를 높이면 반응평형은 효소-기질복합체 형성 쪽으로 기울어져 저해를 받지 않게 된다.(Fig. 9 참조) 효소와 저해제의 결합강도는 저해상수 Ki는 [E][I]/[EI]로 표시된다. 저해제가 존재하면 Vmax은 변화하지 않고 Km은 커진다. 예를들면 다음과 같이 succinate가 fumarate로 되는 반응에서 malonate는 succinate dehydrogenase에 경쟁적 저해제로 작용한다.
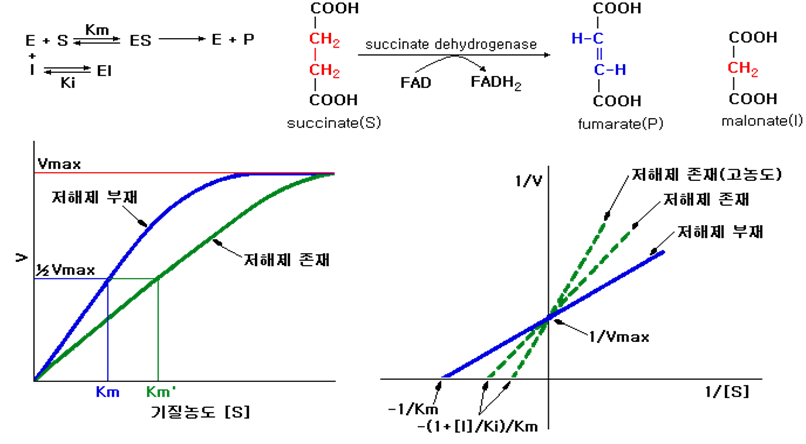 |
| Fig. 9 경쟁적 저해제의 존재에 의한 V와 [S]의 관계 |
- 비경쟁적 저해
비경쟁적 저해(non-competitive inhibition)는 저해제가 유리형의 효소와 효소-기질 복합체 양쪽에 가역적으로 결합하여 저해작용을 나타내는 것이다. 이 저해양식에서는 기질농도 [S]를 높여도 저해가 없어지지 않으며 또 저해제는 기질이 결합하는 부위와는 다른 부위에 결합하여 효소의 활성을 저해하는 것으로 알려져 있으므로 Km은 변화하지 않는다.
저해제 농도가 높아지면 Lineweaver-Burk 직선의 기울기는 커지게 되고 각 직선은 종축상에서 교차하지 않는다.(Fig. 10 참조)
 |
| Fig. 10 비경쟁적 저해제의 존재에 의한 V와 [S]의 관계 |
활성을 나타내는데 SH-기를 필요로 하는 효소에 대한 중금속이온이나 금속이온을 요구하는 효소에 대한 chelate 시약은 흔히 비경쟁적 저해로 된다. 예를 들면 HCN, H2S, CO 등이나 catalase, peroxidase에 대한 Fe, polyphenol oxidase에 대한 Cu, carbonate dehydratase에 대한 Zn, urease나 papain에 대한 Hg, Ag, 산화제(SH-기를 S-S로 하여 불활성화 함), 계면활성제 등이 비경쟁적 저해제이다.
이 저해양식에서 저해상수 Ki는 [E][I]/[EI], Ki'는 [ES][I]/[ESI]로 표시되며 이것은 저해제의 효소 또는 저해제 결합부위로의 친화성을 나타내며 값이 작을수록 친화성이 높다는 것을 의미한다.
- 무경쟁적 저해
무경쟁적 저해(uncompetitive inhibition)는 저해제가 효소-기질 복합체에만 결합하여 효소의 작용을 저해하는 것으로 유리형의 효소와는 결합하지 않는다. 그러므로 기질농도가 증가하여도 저해강도는 영향을 받지 않으며 저해제가 있는 경우에 기질과 효소가 잘 결합한다. 무경쟁적 저해에서는 저해제가 존재하면 Vmax, Km 모두 감소한다.(Fig.. 11 참조) 이 저해양식에서 저해상수 Ki는 [ES][I]/[ESI]로 표시된다.
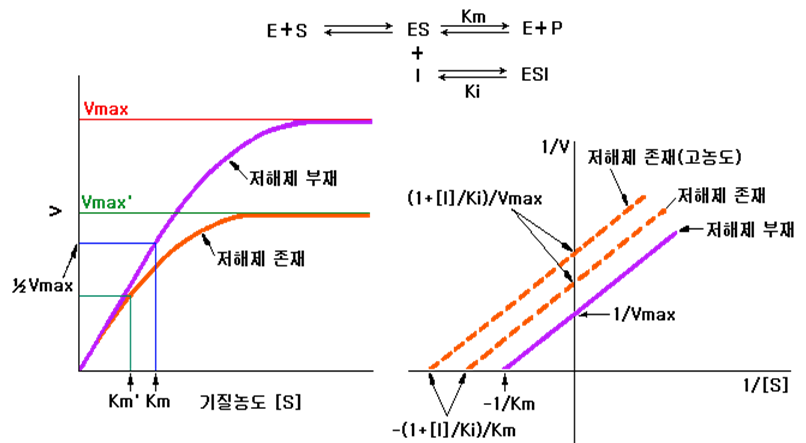 |
| Fig. 11 무경쟁적 저해제의 존재에 의한 V와 [S]의 관계 |
Table 4 가역저해가 존재할 때 효소 반응속도
저해형식 | 반응속도식 | Vmax | Km |
무저해 경쟁적 저해 무경쟁적 저해 비경쟁적 저해 | Vo = Vmax[S]o / (Km + [S]o) Vo = Vmax[S]o / [Km(1+[I]/Ki)+[S]o] Vo = Vmax[S]o / [Km+[S]o(1+[I]/Ki)] Vo = Vmax[S]o / Km(1+[I]/Ki)+[S]o(1+[I]/Ki) | - 불변 감소 감소 | - 증대 감소 불변 |
• 기타 저해
- 최종산물저해
최종산물저해(end product inhibition)는 일련의 대사경로에 있어서 그 경로 초기단계의 효소가 최종산물에 의해 저해를 받는 현상을 말하며 음의 되먹임 저해(negative feedback inhibition)라고도 한다. 생체는 이 방법으로 과잉의 대사산물이 축적하지 않도록 대사를 조절한다. 최종산물이 2 종류 이상인 경우에는 2 종류 이상의 산물이 서로 다른 비율로 저해하거나 동시에 작용할 때에만 저해하며, 또 저해 정도가 다른 몇가지 효소의 존재에 의해 조절된다. 일반적으로 되먹임 저해를 받는 효소는 자신의 기질과 구조가 다른 화합물에 의해 저해받는 allosteric 효소인 경우가 많다.
- 기질저해
효소반응에 있어서 기질농도를 높이면 반응속도가 어떤 최대치에 도달한다음 감소하는 경우를 말하며 이것도 일종의 경쟁적 저해이다.
9) 효소의 활성화
효소의 활성화에는 효소전구체(zymogen)의 활성화, 온도, pH, 용매의 이온강도 등과 같은 비특이적 인자나 보조인자에 의한 활성화, 부활제 또는 활성화제(특정 금속이온 또는 SH-기 보호작용이 있는 cysteine, glutathione, 2-mercaptoethanol 등)에 의한 활성화, allosteric 활성화제(양의 effector)에 의한 활성화 등이 있다.
화합물 첨가에 의한 외견상의 활성화는 단순히 효소실활 방지나 저해제 제거로 작용하는 경우도 있으므로 주의할 필요가 있다.
10) 다기질 반응
2가지 이상의 기질을 필요로 하는 효소반응의 경우 기질이 효소에 결합하고 생성물이 효소로부터 떨어져 나가는 순서가 문제가 된다. 이러한 다기질반응을 촉매하는 효소의 반응형식과 반응기구는 다음과 같이 3가지 형식으로 나타난다.
• 질서적 기구
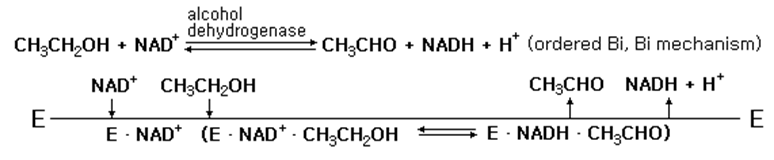
질서적 기구(ordered mechanism)는 효소의 활성부위에 여러가지의 기질이 일정한 순서에 따라 모든 기질이 결합하여야 생성물이 생성되는 경우를 말한다. 이 반응기구의 예로서는 NAD+를 선행기질로 하는 탈수소효소가 있으며 후속기질이 탈수소되어 생성물이 만들어진다. 생성물의 해리는 순서적으로 일어나지 않아도 된다.
• 무질서적 기구
무질서적 기구(random mechanism)는 생성물이 1개라도 생성되기 위해서는 모든 기질이 효소의 활성부위에 결합하여야 할 때, 기질의 결합과 생성물의 분리에 순서가 없는 경우의 기구를 말한다. 이 기구로 반응이 진행되는 효소로서는 여러가지의 phosphotransferase가 있다. 예를 들면 creatine kinase의 경우 기질인 ATP와 creatine은 어느 것이라도 선행기질이 될 수 있으며 3중복합체가 형성된 다음 반응생산물인 ADP와 phosphocreatine가 생성된다. Glycogen을 가수분해하는 phosphorylase도 같은 기구를 가진다.
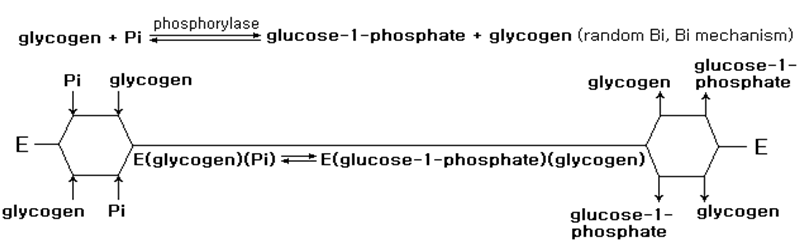
• 핑퐁기구
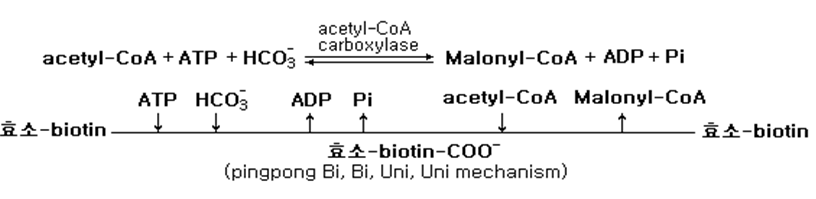
핑퐁기구(pingpong mechanism)는 효소가 먼저 기질과 효소-기질 복합체를 형성하고 다음에 복합체가 생성물을 방출하는 순서에 따라 새로운 기질과 결합하여 최종생성물을 생성하는 기구를 말한다.
이 기구는 모든 기질이 결합하기 전에 반응생산물의 일부가 유리하는 반응형식이다. 이 기구에 의해 반응을 일으키는 효소는 acetyl-CoA carboxylase, aspartate aminotransferase 등이 있다.


!&emoji=☕&slug=xFu35q9&button_colour=5F7FFF&font_colour=ffffff&font_family=Poppins&outline_colour=000000&coffee_colour=FFDD00)



![[일반생물학실험]온도와 pH가 효소작용에 미치는 영향 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjdvNA5S925m8lScjFhJj-uy5SdCcaNFG1AuR_7BbQbDEoHBDEEkqfM64sipvro3RydmSO4_MS2794o2bJ0FCljQ31pcD5W39ZGOHROD7qKXLO1rlm2ZuBtbxJ9CZHSnsk2v1KSEsL4EGA/w680/%25EC%2598%25A8%25EB%258F%2584%25EC%2599%2580+pH%25EA%25B0%2580+%25ED%259A%25A8%25EC%2586%258C%25EC%259E%2591%25EC%259A%25A9%25EC%2597%2590+%25EB%25AF%25B8%25EC%25B9%2598%25EB%258A%2594+%25EC%2598%2581%25ED%2596%25A5.PNG)
![[일반생물학실험]여러 조건에 따른 효소 반응](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj4kaETe9N8j9q9-ClYy9V1kM2L9s5l19K6YoBOE0SB70BmssQXzVADvQijp1ieiQ9mIxcmCwz9e-YCQFVnXYR7m1vmfjTSs0ZNxCmBLG7wgzRBqiY1Kizx8YuhSdw-RDbs1PohokUd69c/w680/%25EC%2597%25AC%25EB%259F%25AC+%25EC%25A1%25B0%25EA%25B1%25B4%25EC%2597%2590+%25EB%2594%25B0%25EB%25A5%25B8+%25ED%259A%25A8%25EC%2586%258C+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반생물학실험]항생제 감수성 검사 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEhwCJEjB_r2Ojsrn244q-fQmpHsDyUUfgWMUnsfhPKQeN2e7_u1pN_ZuwIdxPLVWS6LFywJUrDTYWJe2V6ZVVb1PtfyvX62Y15OxPfXoiaJkqVoSir3ZoFAmDpe5GcoMBmxEsJUKsSvWYc/w680/%25ED%2595%25AD%25EC%2583%259D%25EC%25A0%259C+%25EA%25B0%2590%25EC%2588%2598%25EC%2584%25B1+%25EA%25B2%2580%25EC%2582%25AC.PNG)
![[고분자공학실험]PMMA 중합 반응 - MMA, AIBN 정제와 PMMA Bulk 중합 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj5hkRZhYWcXolP679_yO0kyP8_R-G9dlTqk5AGEdfsIq9M5K3DJc_tvpYck4x1kciBm2IWwFygrzfWH-HPzUjXiCHAFrjv9zeKYDxAl2tGNqgryyc3t9y4B9lQveS_coAqnmZw4pX4Hyo/w680/PMMA+%25EC%25A4%2591%25ED%2595%25A9+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반화학실험]산화-환원 적정 : 비타민 C의 정량 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEintFUW1pYHbKK8MPzki4vdqVMjTUEFFxPdZB1sTJQw13XSFZWqcN5w0x1AlyzfErlYYSgoNqBni4YGlpFC4ZeULK9VHbhfIXLiuZ3UWTl2oBRua7FE8UUQqtYEx3498FENAnlHlh0f8RFkT7Na8jveOtBtQ5UbY8jE80ZCwFoU_jqw_0Z6BofRYZF7/w680/%EC%82%B0%ED%99%94-%ED%99%98%EC%9B%90%20%EC%A0%81%EC%A0%95%20-%20%EB%B9%84%ED%83%80%EB%AF%BC%20C%EC%9D%98%20%EC%A0%95%EB%9F%89.PNG)
0 댓글