수용성 비타민(Water-soluble Vitamins) -1
수용성 비타민은 물에 녹는 비타민이다. 과잉섭취 시 체내에 축적되지 않고 배설되기 때문에 몸 안에 독은 되지 않는다 수용성 비타민의 종류로 비타민B군, 비타민C, 비오틴, 엽산, 콜린, 이노시톨 등이 있다.
1) Vitamin B1(thiamin) Group
처음 thiamine에 대해서 연구하던 학자들은 다발성 신경염에 걸려있는 닭을 쌀겨로 치료하였다고 한다. 즉 thiamine의 부족은 신경염의 원인이 된다는 것을 알게 되었다. 그래서 초창기에는 aneurin(antineuritic)이라 불렀으며 현재도 aneurin이라는 명칭도 사용한다. Thiamine 이란 용어는 Vitamin B1의 작용을 하는 모든 물질에 대한 이름이다. 구조적으로 Vitamin-B1의 분자는 음이온을 갖게 되는데 어떤 종류의 음이온이든 상관이 없다. 즉 양이온분자 부분이 thiamine의 특성을 갖는 부분이며, A의 부분은 어떤 종류의 음이온도 가능하나 보통은 chloride이다.
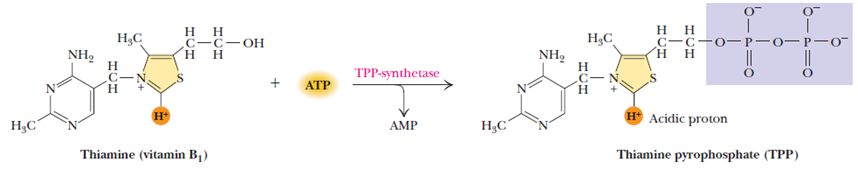
Thiamine은 무색의 결정체이며 특유의 냄새와 약간의 쓴맛을 낸다. 수용성으로 alcohol과 아세톤에 약간 녹으며 에텔, 벤젠, 핵산, 클로로포름등 유기용매에는 불용성이다. 산성용액에서는 안정하며 가열해도 파괴되지 않지만, 중성이나 알카리성용액에서는 산화되어 thiochrome이라는 형광물질로 변하며 생물학적으로 불활 성화된다. 순수한 Vitamin B1은 공기중에서 쉽게 산화되지 않는다. 상업적으로 이용되는 Vitamin B1 제제 hydrochloride form 보다는 안정도가 높은 mononitrate form을 더 많이 활용한다. Thiamine은 열, 알카리, 산소, 방사선에 불안정하다.
비타민 B1(thiamin)은 항각기인자, 항신경염인자로 알려져 있는 수용성 비타민이다. 생체내에는 대부분이 thiamin pyrophosphate(TPP)로 존재하고 그 외에 유리 thiamin, thiamin monophosphate(TMP), thiamin triphosphate(TTP), 그리고 근육 중에 hydroxyethylthiamin(HET)으로 존재하며 TMP나 TTP는 보효소 기능이 없다.(Fig. 1)
Thiamin pyrophosphate는 체내에서 Mg2+와 복합체를 형성하여 당질대사에 관련된 여러 가지 효소의 보효소로 작용한다. 즉 pyruvate dehydrogenase와 α-ketoglutarate dehydrogenase의 산화적 탈탄산반응과 transketolase 반응 등에서 보효소로 작용한다. 또 분지아미노산에서 생성된 α-케토산의 산화적 탈탄산반응에도 관여하며 미생물에서는 pyruvate decarboxylase 등의 비산화적 탈탄산반응 효소의 보효소가 되기도 한다.
비타민 B1이 결핍되면 각기증(beriberi)이라는 다양한 증상의 질환이 일어난다. 이 것의 증상으로 다발성신경염에 의한 지각둔화, 기억장해, 운동마비, 건반사 이상, 시신경염, 안근마비, 항근마비, 배복근 악통과 같은 신경 및 근 증상이 나타난다. 이외에 심확대, 우심부전, 제 2 폐동맥음 항진, 부정맥, 심전도 이상과 같은 순환기계 증상, 부종 그리고 식욕부진, 변비, 소화관 이완과 같은 소화기증상이 나타난다. 비타민 B1은 동물에는 각종 조직세포에 균일하게 함유되어 있고 식물에는 종자의 배아에 유리형으로 많이 함유되어 있으며 특히 효모세포에 다량으로 함유되어 있다.
 |
R = -H, R = -Pi, R = -PiPi, R = -PiPiPi thiamin, thiamin monophosphate(TMP), thiamin pyrophosphate(TPP), thiamin triphosphate(TTP) Fig. 1 Thiamin과 그 유도체 |
2) Vitamin B2(riboflavin) Group
Riboflavin은 Vitamin-G, lactoflavin, ovoflavin 등 여러가지 이름으로 불리어왔다. B-그룹 비타민들의 특징인 형광과 우유와 계란노른자에서와 같은 색상을 나타낸다. 노란단백질효소로 인체의 대사 및 건강에 필수성분인 flavin색소이다. 수용성인 riboflavin은 주로 소변으로 배설되므로 vitamin을 섭취한 후 소변이 노랗게 되는 것은 riboflavin때문이다.
노란색의 분말로 가벼운 냄새를 갖고 있다. 건조상태에서는 빛에 노출되어도 비교적 안전하나, 용액상태에서 특히 알카리성 용액에서는 빠른 속도로 변질되고 이때에 빛이 가해지면 더 가속화된다. 알칼리용액에서는 쉽게 용해되지만 열과 광선에 불안정하여 lumiflavin이란 물질로 되는데 이는 생물학적 활성을 잃는 것이다. Rivoflavin은 pH 1.0~6.5의 산성용액에서는 열에는 안정하나 광선아래서는 lumichrome이란 물질로 되면서 활성을 잃는다. Riboflavin의 수용액은 황녹색의 형광을 나타낸다. 수용액은 hydrosulfite나 hydrogen에 의해 zinc를 촉매로 무색, 무형광의 leucoriboflavin으로 바뀐다. Leuco-riboflavin은 공기중에서 흔들면 다시 쉽게 산화된다.
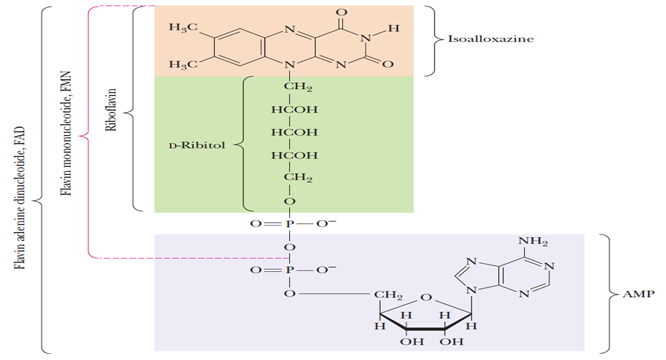 |
The structures of riboflavin, flavin mononucleotide (FMN), and flavin adenine dinucleotide (FAD). Flavin coenzymes bind tightly to the enzymes that use them, with typical dissociation constants in the range of 10-8 to 10-11 M, so that only very low levels of free flavin coenzymes occur in most cells. Even in organisms that rely on the nicotinamide coenzymes (NADH and NADPH) for many of their oxidation–-reduction cycles, the flavin coenzymes fill essential roles. Flavins are stronger oxidizing agents than NAD+ and NADP+. They can be reduced by both one-electron and two-electron pathways and can be reoxidized easily by molecular oxygen. Enzymes that use flavins to carry out their reactions—- flavoenzymes—-are involved in many kinds of oxidation–-reduction reactions |
비타민 B2는 쥐의 성장촉진인자로 알려져 있으며 동물조직에는 대부분 FAD (flavin adenine dinucleotide)나 FMN(flavin mononucleotide)으로 존재하고 장관에 가장 많이 분포되어 있다. 유리형은 우유, 난황, 난백, 망막, 피부, 요 중(대부분 FMN)에 존재한다. 생리작용으로는 mitochondria나 microsome 내의 flavoprotein이나 산화효소(oxidase), 탈수소효소(dehydrogenase), 산소첨가효소(oxygenase) 등의 산화환원효소내에 보결분자족으로 함유되어 있으며 flavin의 산화 환원에 의해 수소 및 전자의 전달에 관여한다. Flavin 효소 중에는 Fe, Mo 등의 금속을 함유하는 것도 있는데 이들을 금속 flavoprotein이라 한다.
 |
Fig. 2 Riboflavin, FMN 및 FAD의 구조 |
항생물질, 신경안정제, 부신피질호르몬을 투여하거나 간질환, 당뇨병, 하수체질환 등으로 비타민 B2 결핍증이 나타나는 경우가 있다. 그 원인은 약제와 복합체 형성, 장내세균군의 합성 저하, 흡수불량, 보효소 합성억제, 체내 소비증가, 아포효소 생성 장해, 효소반응 저해 등이다. 결핍증은 피부점막 증상으로 구각염, 구순염, 설염, 지루성 습진, 결막염, 수명(羞明), 피부염, 각막주변 혈관증가, 미만성 표층각막염 등이 나타난다. 간, 우유, 난황, 난백, 효모, 배아 등에 많이 함유되어 있으며 1일 권장량은 5~10㎎이다.
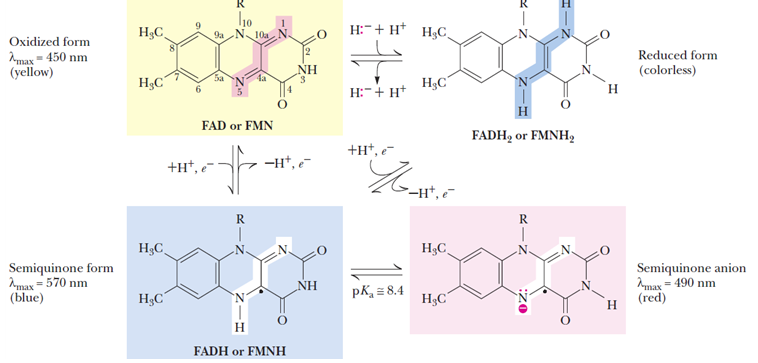 |
The redox states of FAD and FMN. The boxes correspond to the colors of each of these forms. The atoms primarily involved in electron transfer are indicated by red shading in the oxidized form, white in the semiquinone form, and blue in the reduced form |


!&emoji=☕&slug=xFu35q9&button_colour=5F7FFF&font_colour=ffffff&font_family=Poppins&outline_colour=000000&coffee_colour=FFDD00)



![[일반생물학실험]온도와 pH가 효소작용에 미치는 영향 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjdvNA5S925m8lScjFhJj-uy5SdCcaNFG1AuR_7BbQbDEoHBDEEkqfM64sipvro3RydmSO4_MS2794o2bJ0FCljQ31pcD5W39ZGOHROD7qKXLO1rlm2ZuBtbxJ9CZHSnsk2v1KSEsL4EGA/w680/%25EC%2598%25A8%25EB%258F%2584%25EC%2599%2580+pH%25EA%25B0%2580+%25ED%259A%25A8%25EC%2586%258C%25EC%259E%2591%25EC%259A%25A9%25EC%2597%2590+%25EB%25AF%25B8%25EC%25B9%2598%25EB%258A%2594+%25EC%2598%2581%25ED%2596%25A5.PNG)
![[일반생물학실험]여러 조건에 따른 효소 반응](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj4kaETe9N8j9q9-ClYy9V1kM2L9s5l19K6YoBOE0SB70BmssQXzVADvQijp1ieiQ9mIxcmCwz9e-YCQFVnXYR7m1vmfjTSs0ZNxCmBLG7wgzRBqiY1Kizx8YuhSdw-RDbs1PohokUd69c/w680/%25EC%2597%25AC%25EB%259F%25AC+%25EC%25A1%25B0%25EA%25B1%25B4%25EC%2597%2590+%25EB%2594%25B0%25EB%25A5%25B8+%25ED%259A%25A8%25EC%2586%258C+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반생물학실험]항생제 감수성 검사 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEhwCJEjB_r2Ojsrn244q-fQmpHsDyUUfgWMUnsfhPKQeN2e7_u1pN_ZuwIdxPLVWS6LFywJUrDTYWJe2V6ZVVb1PtfyvX62Y15OxPfXoiaJkqVoSir3ZoFAmDpe5GcoMBmxEsJUKsSvWYc/w680/%25ED%2595%25AD%25EC%2583%259D%25EC%25A0%259C+%25EA%25B0%2590%25EC%2588%2598%25EC%2584%25B1+%25EA%25B2%2580%25EC%2582%25AC.PNG)
![[고분자공학실험]PMMA 중합 반응 - MMA, AIBN 정제와 PMMA Bulk 중합 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj5hkRZhYWcXolP679_yO0kyP8_R-G9dlTqk5AGEdfsIq9M5K3DJc_tvpYck4x1kciBm2IWwFygrzfWH-HPzUjXiCHAFrjv9zeKYDxAl2tGNqgryyc3t9y4B9lQveS_coAqnmZw4pX4Hyo/w680/PMMA+%25EC%25A4%2591%25ED%2595%25A9+%25EB%25B0%2598%25EC%259D%2591.PNG)
![[일반화학실험]산화-환원 적정 : 비타민 C의 정량 1부](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEintFUW1pYHbKK8MPzki4vdqVMjTUEFFxPdZB1sTJQw13XSFZWqcN5w0x1AlyzfErlYYSgoNqBni4YGlpFC4ZeULK9VHbhfIXLiuZ3UWTl2oBRua7FE8UUQqtYEx3498FENAnlHlh0f8RFkT7Na8jveOtBtQ5UbY8jE80ZCwFoU_jqw_0Z6BofRYZF7/w680/%EC%82%B0%ED%99%94-%ED%99%98%EC%9B%90%20%EC%A0%81%EC%A0%95%20-%20%EB%B9%84%ED%83%80%EB%AF%BC%20C%EC%9D%98%20%EC%A0%95%EB%9F%89.PNG)
0 댓글